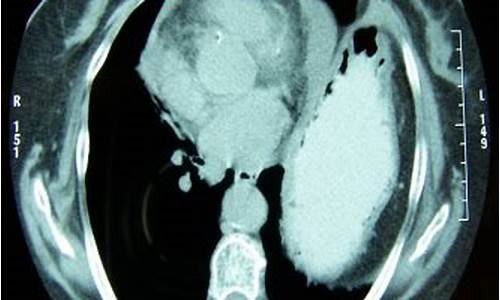
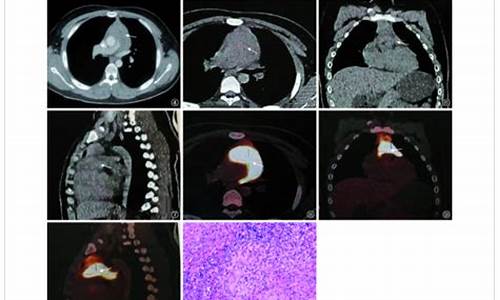
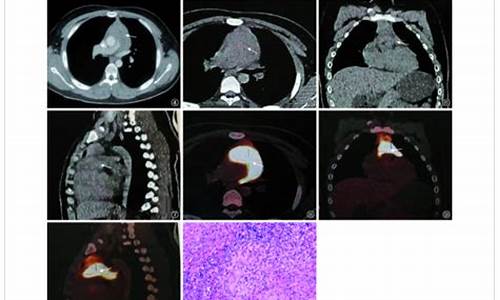
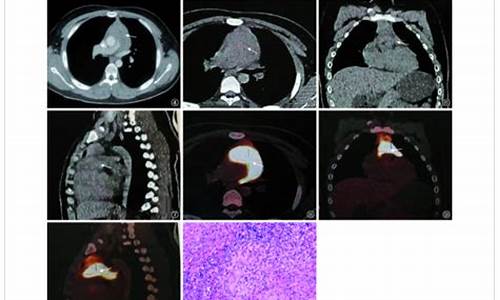
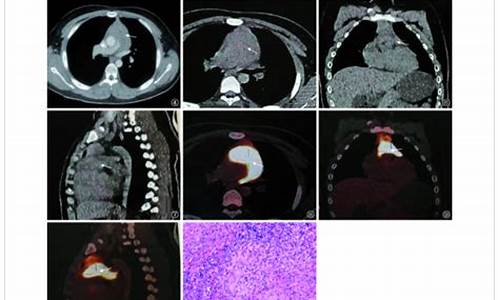
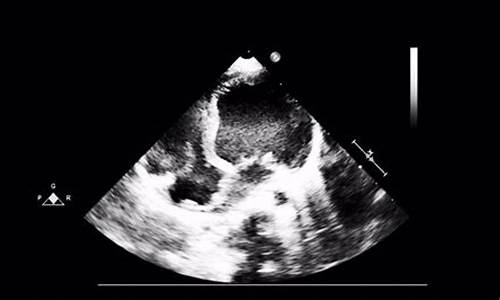
心包结核病例有哪些类型的_心包结核怎么确诊
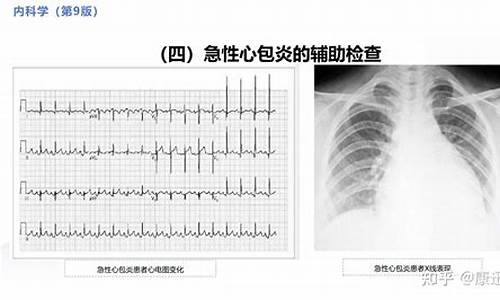
心包疾病谱包括先天性心包缺如、心包炎(干性、渗出性、渗出-缩窄性与缩窄性)、肿瘤性与囊肿。病因学分类包括:感染性、全身自身免疫疾病伴心包炎、2型自身免疫疾病、邻近器官疾病伴心包炎、代谢疾病伴心包炎、妊娠合并原因不明心包积液(少见)、外伤性心包炎、肿瘤性心包疾病(原发性、继发性)等。 在胚胎时期原始腔隙未能和其他腔隙隔合成心包,而单独形成一个空腔,以后就可发展成为心包囊肿。囊肿壁多菲薄透明,外壁为疏松结缔组织,内壁为单层的间皮细胞,其上有血管分布,类似心包组织,囊内含有澄清或淡**液体,偶见血性液体。心包囊肿比较少见,约占纵隔肿瘤与囊肿的8.9%,纵隔囊肿的17%。其发病率较低的原因,除本病少见外,尚因多数无症状,有的囊肿小又与纵隔阴影互相重叠,不易被发现,发病年龄多为青壮年。多数患者无自觉症状,多为其他原因胸部偶然发现,有症状者为心悸、气短、咳嗽及心前区不适,也有患者可查见心电图异常,可能与肿物压迫有一定关系。少数病例因囊肿压迫膈神经而使患侧季肋部痛,并向肩部放射,疑似慢性胆囊炎;有的病例可因过劳或体位改变而使疼痛加剧;如果囊肿发生破裂可并发炎症表现。
胸部X线检查在心膈角处有明显阴影,深呼吸和体位改变可见阴影形态和大小都有明显改变。 适应证、禁忌证与方法
1.在心包穿刺术项下指南首次指出主动脉夹层伴心包积血是心包穿刺的禁忌证(可使夹层血肿扩大),该类病人应立即进行手术治疗。
2.指南建议应尽可能在心导管室X线与心电图监视下做心包穿刺,因常用的穿刺针连接心电图导联记录心包腔内心电图并不能提供足够的安全保障。3.建议用剑突下径路,以防损伤胸膜、冠状动脉与乳内动脉。
4.每次抽液量不应超过1L,以防急性右室扩张。
5.急性心脏压塞为争取时间可在超声引导下行心包穿刺引流。
6.如需持续引流,可经软性J字形导丝引入扩张管,然后插入多孔猪尾巴导管(导丝位置应通过两个投射位确认),待心包引流液小于25ml/d时拔除导管。
7.外伤性心包积血与化脓性心包炎均应及时作外科引流。
8.对心包积液量较少(200~300ml或<200ml)者使用切线进路侧位观察心外膜晕轮现象可增加穿刺成功率并减少并发症。 1.除常规检查、培养与找癌细胞外,对疑有恶性肿瘤者应测定CEA,AFP,糖类抗原CA125,CD-30,CD-25等。
2.CEA增高,ADA(腺苷脱氨酶)降低可鉴别肿瘤与结核。
3.对结核诊断,PCR敏感性与ADA相似,但前者特异性更高。
4.对疑有细菌感染者,应同时做心包液与周身血液厌氧需氧菌培养三次。
5.亲心脏PCR分析可协助鉴别性或自身免疫性心包炎(证据B,II a类)。6.化脓性积液中葡萄糖值显著降低。
7.WBC计数极低支持粘液水肿;单核细胞显著增高支持恶性肿瘤或甲状腺功能减退;类风湿病或细胞感染者中性粒细胞均可增高。
8.与细菌培养相比,Gram染色特异性虽高(99%),但敏感性仅38%。
9.联合测定上皮膜抗原、CEA与波形蛋白免疫细胞化学染色可协助鉴别反应性间皮细胞与腺癌细胞。 1.病程大于三个月者称慢性心包炎。
2.除非合并心脏压塞,否则症状很轻或无症状(疲倦、心悸、胸部不适)。
3.对反复发作的症状性患者应进行球囊心包切开或心包切除治疗(证据B,II b类指征)。 1.复发性心包炎包括以下类型:①间歇发作性;②持续性。
2.有以下表现者支持有免疫功能障碍:①潜伏期持续数月;②存在抗心脏抗体;③类固醇激素治疗很快显效且同时存在其它自身免疫性疾病如红斑性狼疮等。3.非甾体类抗炎药、皮质激素治疗无效时可试用秋水仙碱以预防复发,推荐剂量为2mg/d治疗一或两天,随后1mg/d(证据B,I类指征)。皮质激素仅适用于严重病例。1~1.5mg/ kg·d),至少使用一个月,如效果不佳可并用硫唑嘌呤(75~100mg/d)或环磷酰胺。皮质激素起始剂量应大,减量应慢,在减至一定维持量时可合用秋水仙碱或非甾体类抗炎药,以防症状反跳。难治性重症病例可行心包切除术,术前应先停用皮质激素数周。 1.强调指出,快速积聚的少量积液或积血可发生急性心脏压塞,主要症状是低血压或休克,而缓慢积聚的大量积液却可无明显症状。前者可称为“外科性”压塞,大多由心包出血或积血引起,后者称“内科性”压塞,大多由炎症引起。
2.无炎症改变(典型胸痛、心包摩擦音、发热、弥漫性ST段抬高)的心脏压塞多为恶性积液。
3.心包内积血与血栓形成时典型超声透光区可消失,故可漏诊心脏压塞。经食管超声检查可揭示真相。
4.低血容量、心动过速可促发心包积液病人出现心脏压塞,故应及时治疗。
5.快速静脉输液可暂时性缓解急性心脏压塞症状,但一旦诊断应立即作心包穿刺引流。 1.过去认为心包增厚是诊断缩窄性心包炎的必要诊断条件,但Mayo医院外科大组手术病例分析显示18%缩窄性心包炎病人并无心包增厚。
2.缩窄性心包炎的主要表现是疲倦、气短、末梢水肿与腹胀,失代偿期患者才有静脉淤血、肝肿大、胸腔积液与腹水。
3.鉴别限制性心肌病与缩窄性心包炎的最佳方法是通过多普勒超声测定在前负荷改变或不改变时的呼吸周期改变[3]、MRI或CT亦有帮助。
4.弥漫性严重钙化粘连者外科手术危险性高,且易损伤心脏,另一方法是使用激光切削术。可适当保留严重钙化与瘢痕区,以防过度出血。影响预后的因素主要是心肌广泛纤维化与萎缩,故应争取尽早手术。 一、性心包炎
1.为欧洲最常见的心包炎病因,可为直接侵犯或免疫反应的结果。
2.心包积液和/或心包活组织检查是确诊性心包炎的必要条件,这主要依据PCR或原位杂交技术(证据B,II a类指征)。血清抗体滴度增加4倍可提示但不能确诊性心包炎(证据B,II b类指征)。
3.指南指出性心包炎禁用皮质激素治疗,推荐使用干扰素或免疫球蛋白。
二、细菌性心包炎
1.细菌性心包炎或化脓性心包炎大多源于身体其它部位感染或败血症,一旦怀疑或确诊细菌性心包炎应即进行心包穿刺与送验。
2.本病应在全身使用抗生素控制感染情况下,优先考虑经剑突下行心包切开,以彻底引流,并同时切除增厚的心包;仅轻症病例可施行猪尾巴导管持续引流并灌注抗生素与尿激酶。
三、结核性心包炎
1.临床表现呈多样性,诊断主要依据心包液或组织中找到分枝杆菌和/或有干酪样肉芽肿。
2.PCR测定可在<1ml的心包液中辨认结核分枝杆菌的DNA。
3.心包液γ干扰素与腺苷脱氨酶浓度升高亦有较高的诊断价值。
4.心包活检比心包液诊断敏感性高,有助于快速诊断。
5.结核菌素皮肤试验阴性率可达25%~33%,阳性率亦达30%~40%,故诊断价值不大。
6.结核性心包积液呈三高现象:高比重、高蛋白含量与高白细胞计数(0.7~54×109/L)。
7.抗结核的联合药物治疗仅适用于确诊或高度可疑病例。
8.一项荟萃分析显示,联合使用皮质激素可减少手术治疗的需求与降低死亡率(证据A,II b类指征)。如果使用,那么的用量必须相对要大[1~2mg/(kg·d)],这是因为利福平可以增强皮质激素的肝脏代谢。上述剂量应用5~7天,然后逐渐减量,疗程为6~8周。
9.经上述治疗仍出现心包缩窄表现者,应尽早手术治疗(证据B,I类指征)。 1.增强CT或CT与淋巴管造影结合可对胸导管部位作出定位并显示淋巴管与心包的连接部位。
2.心胸手术后的乳糜心包可用心包穿刺与进食中链甘油三酯治疗,内科治疗失败者可施行心包-腹膜开窗术;对胸导管径路可精确定位者,可在横隔上进行结扎与切除。
声明:本站所有文章资源内容,如无特殊说明或标注,均为采集网络资源。如若本站内容侵犯了原著者的合法权益,可联系本站删除。